Новое исследование позволяет заключить, что антибиотикотерапия может быть причиной бессимптомного течения нозокомиальной (госпитальной) инфекции, вызываемой патогеном Clostridium difficile. Группа исследователей из Института Сэнгера в Великобритании (Wellcome Trust Sanger Institute) успешно воспроизвела инфекционный цикл данного возбудителя в условиях эксперимента на мышах посредством создания условий, аналогичных тем, при которых происходит заражение человека. Результаты исследования имеют значение для методов контроля инфекции в госпитальных условиях и открывают двери для усовершенствования лечения и диагностики заболеваний, вызываемых C. difficile.
В настоящее время тактика лечения заболеваний, чьим этиологическим фактором является C. difficile, основана на строгом соблюдении гигиенических правил и изоляции лишь пациентов с симптомами инфекции – диареей и повышенной температурой. Но данное сообщение говорит о необходимости включения в поле госпитального контроля всех пациентов, проходящих курс антибиотикотерапии.
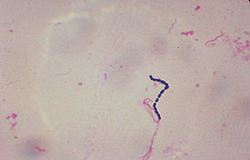
«C. difficile] – чрезвычайно вирулентный и резистентный патоген, устойчивый к широкому спектру антибиотиков. До недавнего времени опыты на животных фокусировались на острых симптомах заболевания, вызываемого C. difficile. Однако для понимания путей распространения этого патогенного микроорганизма необходимо знание его полного цикла развития. Мы наблюдали за мышами, инфицированными C. difficile, и обнаружили, что они выделяли незначительное количество спор и не инфицировали других мышей», - объясняет доктор Тревор Лаули (Trevor Lawley), руководитель исследований из Института Сэнгера. – «Но когда мы вводили мышам антибиотики, то наблюдалось поразительное увеличение количества выделяемых ими спор и заражение остальных животных. Важно отметить, что распространение инфекции имело место даже в случае отсутствия клинических симптомов у экспериментальных объектов».
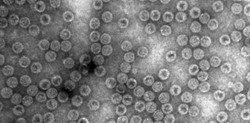
Распространение инфекции происходит путем выделения человеком высоко резистентных спор. Бактериальные споры представляют собой, по сути дела, дормантные клетки (клетки в состоянии покоя) с внешними защитными оболочками, делающими их хорошо приспособленными к выживанию и распространению в различных условиях окружающей среды. После выделения споры способны при неблагоприятных условиях и высокой температуре (выше 70 градусов Цельсия) находиться в состоянии покоя в течение длительного времени, пока не произойдет инфицирование нового человека.
«Мы проводили мышам курс короткой и длительной антибиотикотерапии. Спустя две недели по окончании короткого курса у большинства мышей происходило уменьшение количества выделяемых спор, но по завершении длительного применения антибиотиков некоторые мыши достаточно долго продолжали выделять споры в избыточном количестве. На основании этих результатов мы должны понимать, что те пациенты, у которых отсутствуют клинически выраженные симптомы инфекции, вызываемой C. difficile, представляют собой значительную угрозу заражения других людей в течение нескольких недель после прекращения приема антибиотиков», - говорит профессор Гордон Дауган (Gordon Dougan), руководитель отдела генетики патогенных микроорганизмов Института Сэнгера и главный автор данного исследования.
Ученые также установили, что существует значительная опасность заражения и из окружающей среды. Даже при кратковременном пребывании в клетках мышей, обильно выделяющих споры, происходила контаминация среды, приводящая к инфицированию интактных животных. Это говорит о том, что даже незначительное обсеменение среды представляет собой потенциальную инфекционную опасность.
Применение антибиотиков – фактор риска в развитии инфекции C. difficile. Как известно, в желудочно-кишечном тракте здорового человека находится природное сообщество различных симбионтных микроорганизмов, играющих важную роль в нормальном функционировании организма хозяина.
Когда исследователи вводили мышам антибиотики, баланс микробной экосистемы нарушался. Поскольку клетки C. difficile резистентны ко многим антибиотикам, то они получали преимущества для размножения, в отличие от естественной микрофлоры желудочно-кишечного тракта, погибающей в результате действия антибиотиков. Это позволяло данному микроорганизму доминировать в микробиоте мышей и неограниченно размножаться.
Несмотря на то, что у большинства мышей отсутствовали выраженные симптомы заболевания, исследователи установили, что мыши с мутацией, ассоциированной с ослаблением иммунитета, теряли в весе и погибали в результате заражения. Схожесть с острым течением инфекции C. difficile у пожилых или с ослабленной иммунной защитой людей позволяет использовать мышиную модель как адекватный способ изучения госпитального заражения пациентов данным патогеном.
Было показано, что споры C. difficile могут быть изолированы и очищены посредством водной промывки. Этот способ позволяет сохранять их природные свойства и устойчивость к широкому спектру факторов окружающей среды, а также делает возможным использование в экспериментальных целях и для установления их структуры.
«C. difficile – высоко специализированный патоген, повинный в смертности пациентов наших госпиталей, но его биология и способ распространения еще мало изучены», – говорит Брендан Врен (Brendan Wren), профессор микробного патогенеза Лондонской Школы гигиены и тропической медицины Департамента инфекционных и тропических болезней (London School of Hygiene & Tropical Medicine's Department of Infectious & Tropical Diseases). – «Теперь мы можем прослеживать циркуляцию этого опасного микроорганизма, используя простую модель. Это важно для определения роли спорообразования в передаче инфекции и понимания того, как и почему некоторые штаммы C. difficile являются более вирулентными и контагиозными, чем другие. Кроме того, использование модели облегчает установление роли факторов организма-хозяина в развитии заболевания и способствует лучшей диагностике и стратегии лечения с целью снижения тяжести вызываемых C. difficile заболеваний».
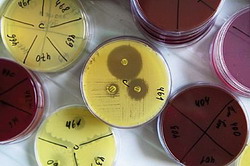
Отрабатывая методики выделения спор и механизм передачи C. difficile у мышей, исследователи одновременно тестировали дезинфектанты, традиционно используемые в госпиталях. Спиртосодержащие дезинфектанты не обладали активностью по отношению к данному микроорганизму. В то же время 20-минутная обработка поверхности спороцидным агентом приводила к снижению степени контаминации среды и приостанавливала циркуляцию возбудителя.
Данные исследования служат очередным шагом в направлении уменьшения проблем здравоохранения, проявляющихся в десятикратном увеличении случаев C. difficile за последнее десятилетие. В 2007 году в Великобритании имели место 56 000 таких случаев, в то время как за первые три месяца 2009 года отмечено снижение их количества по сравнению с тем же периодом 2008 года. Наибольшую проблему представляют псевдомембранозные колиты – инфекционные заболевания толстой кишки, часто завершающиеся летальным исходом для пациентов с ослабленным иммунитетом.
«Значение результатов данного исследования заключается в лучшем понимании взаимодействий между C. difficile, микробиотой кишечника и иммунной системой хозяина в ответ на введение антибиотиков. Это открывает широкие возможности, включая разработку и применение новых пробиотиков, которые могут восстанавливать баланс кишечной микрофлоры и улучшать здоровье. Данное исследование имеет значение для улучшения лечения и инфекционного контроля заболевания, представляющего все возрастающую глобальную опасность для здравоохранения всего мира», - говорит доктор Фиона Куок (Fiona Cooke), сотрудница Департамента медицинской микробиологии при Адденбрукском госпитале в Кембридже (Department of Medical Microbiology at Addenbrooke's Hospital, Cambridge).